Epigenetica is een hot topic in het onderzoek naar erfelijkheid. Het bestudeert overerfbare eigenschappen die niet direct in het DNA zijn vastgelegd, en dit veld is nog volop in ontwikkeling. Desondanks zijn er al medicijnen die ingrijpen op het epigenoom.
De Evolutie van Erfelijkheidsonderzoek
Tien jaar geleden was het nog ondenkbaar om te stellen dat verworven eigenschappen overerfbaar zijn. Dit idee deed denken aan de theorie van Jean Baptiste Lamarck, die suggereerde dat giraffehalzen langer werden door het rekken ervan om bij hoge bladeren te komen. Hoewel dit specifieke voorbeeld onjuist is, durven wetenschappers tegenwoordig wel te beweren dat verworven eigenschappen inderdaad kunnen overerven.
Onderzoekers van Duke University toonden aan dat genetisch identieke moedermuizen, door een verschil in dieet, nakomelingen kregen met een andere vachtkleur. Als de zogenaamde agoutimuizen voor en tijdens de zwangerschap veel foliumzuur aten, resulteerde dit in donkerbruine nakomelingen in plaats van lichtbruine. Dit leek aanvankelijk verklaarbaar doordat genen onder invloed van externe factoren staan.
Echter, het verschil in vachtkleur bleek nog generaties stand te houden, zonder enige verandering in de volgorde van het DNA. Dit fenomeen werd toegeschreven aan veranderingen op het niveau van de bouwstenen van DNA, specifiek aan de methylering van cysteïne (C). Bij donkerbruine muizen bleken methylgroepen aan de nucleotiden van het gen dat codeert voor vachtkleur te zijn gebonden, wat leidde tot de inactivatie van dit gen. Deze methylering werd doorgegeven aan het nageslacht, puur door voeding, aangezien foliumzuur rijk is aan methylgroepen.
Tweelingen en Epigenetische Veranderingen
Onderzoek naar DNA-methylatie bij eeneiige tweelingen heeft aangetoond dat de mate van methylering in de loop der jaren sterk verandert. Hoewel een bevruchte eicel een initiële epigenetische code heeft die tijdens de embryonale ontwikkeling grotendeels wordt verwijderd en opnieuw wordt gevormd, laten studies zien dat bij driejarige eeneiige tweelingen het methylatiepatroon nog nagenoeg gelijk is. Bij vijftigjarige eeneiige tweelingen ontstaan echter aanzienlijke verschillen in methylering onder invloed van externe factoren, wat resulteert in variaties in genactiviteit. Hierdoor lijken eeneiige tweelingen na verloop van tijd minder op elkaar.
Het is duidelijk dat epigenetische factoren een cruciale rol spelen bij ontwikkelingsstoornissen zoals het Angelmansyndroom en het syndroom van Beckwith-Wiedemann. Deze aandoeningen worden gekenmerkt door de betrokkenheid van zogenaamde 'imprinted genes'. Bij gezonde individuen is één kopie van zo'n gen, afkomstig van de moeder of vader, gemethyleerd en daardoor inactief. Dit is essentieel om een overdosis van het genproduct te voorkomen. Echter, wanneer er op epigenetisch niveau iets misgaat tijdens de bevruchting en de methylgroepen verdwijnen, kunnen deze aandoeningen ontstaan.
Epigenetica en Reproductieve Geneeskunde
De bovengenoemde ontwikkelingsstoornissen lijken relatief vaker voor te komen na in-vitrofertilisatie (IVF). Er wordt vermoed dat de kunstmatige omgeving van de bevruchting op epigenetisch niveau problemen kan veroorzaken. Onderzoekers van de Vrije Universiteit Amsterdam hebben aangetoond dat retinoblastomen vaker voorkomen bij kinderen die na IVF zijn geboren. Hoewel aanvankelijk werd gedacht dat medicatie gebruikt tijdens IVF de oorzaak was, wordt nu ook geopperd dat epigenetische factoren een rol kunnen spelen.
In vitro fertilisatie (IVF)
De Rol van Epigenetica bij Kanker
Dat epigenetische factoren een rol spelen bij het ontstaan van kanker, zoals retinoblastoom, is niet verwonderlijk. Bij deze vorm van kanker is een tumorsuppressorgen betrokken. Wanneer zo'n gen wordt uitgeschakeld door de binding van een methylgroep, verdwijnt een belangrijke bescherming tegen tumorgroei.
Professor Henk Stunnenberg, hoogleraar moleculaire biologie, benadrukt het belang van epigenetica bij kankeronderzoek. De American Association for Cancer Research stelt zelfs dat er 1 tot 2 miljard dollar nodig is voor onderzoek naar epigenetica.
Stunnenberg coördineert het HEROIC-project (Hightroughput Epigenetic Regulatory Organisation In Chromatin), dat een subsidie van 12 miljoen euro van de Europese Gemeenschap heeft ontvangen. Dit internationale consortium richt zich op methylatie en andere epigenetische factoren. De onderzoeksvraag is of methylering de oorzaak of het gevolg is van ziekte. Door te kijken naar factoren die een primaire rol spelen in epigenetische processen, zoals het aan- en uitzetten van genen, probeert men dit te achterhalen.
Mechanismen van Epigenetische Regulatie
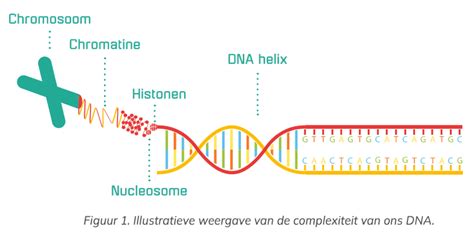
DNA in de cel is verpakt rond eiwitten genaamd histonen, in structuren die nucleosomen worden genoemd. In deze verpakte vorm zijn genen niet afleesbaar. Onderzoek richt zich op de factoren die betrokken zijn bij het 'uitpakken' en weer 'inpakken' van het DNA. Dit proces verloopt via de staarten van histonen, waaraan diverse epigenetische moleculaire verbindingen kunnen hangen. Deze verbindingen fungeren als een soort 'streepjescode' die aangeeft of een gen actief is of niet, afhankelijk van het celtype en de ontwikkeling.
Er zijn ongeveer vijftig bekende modificaties, zoals acetylering, ubiquitinering, methylering en fosforylering. In combinatie met de vier histonen, biedt dit theoretisch miljoenen combinaties. Bepaalde combinaties van modificaties leiden tot genactivatie, terwijl andere tot geninactivatie leiden. Het doel van onderzoek is om de precieze biochemische samenstelling van deze epigenetische laag in kaart te brengen en te bepalen welke 'barcodes' waar op het genoom zijn aangebracht.
HEROIC en ENCODE Projecten
Het HEROIC-project bestudeert het epigenoom van de muis, omdat muizen genetisch gemanipuleerd kunnen worden om de effecten op het epigenoom te onderzoeken. Daarnaast is er het Amerikaanse ENCODE-project (Encyclopedia of DNA Elements), dat zich richt op humane epigenetische factoren.
Epigenetische Behandelingen
Ondanks dat de epigenetica nog in de kinderschoenen staat, wordt er al klinisch onderzoek gedaan naar epigenetische behandelingen. Middelen zoals trichostatine A (TSA) en valproïnezuur (VPA), die de deacetylatie-inhibitie bewerkstelligen, worden onderzocht voor de behandeling van diverse tumoren. Een acetylgroep aan een histonstaart betekent genactivatie, terwijl deacetylering leidt tot inactiviteit. TSA en VPA kunnen dit proces tegengaan.
Hoewel deze middelen nog niet volledig specifiek zijn, blijkt dit bij leukemie geen groot probleem. Kankercellen zijn namelijk hypergevoelig voor interventies op het epigenoom, waardoor met een lage dosis apoptose kan worden veroorzaakt.
Een ander epigenetisch medicijn is azacitidine, goedgekeurd voor de behandeling van myelodysplastisch syndroom. Dit middel kan methylgroepen verwijderen en zo genen reactiveren.
Epigenetica en Diverse Aandoeningen
De epigenetica is van belang bij een breed scala aan aandoeningen, niet alleen kanker en afwijkingen met imprinted genes. Veranderingen in het epigenetische patroon kunnen leiden tot veranderingen in celeigenschappen en daarmee tot ziekte. VPA wordt bijvoorbeeld experimenteel toegepast bij psoriasis vanwege de hyperproliferatie die epigenetisch geblokkeerd kan worden.
Voor aandoeningen die niet gepaard gaan met een verhoogde gevoeligheid voor bestaande epigenetische middelen, is diepgaand onderzoek nodig om specifieke epigenetische afwijkingen te identificeren en gerichte behandelingen te ontwikkelen. Het Angelman-syndroom is hiervan een voorbeeld.
De Toekomst van Epigenoomonderzoek
In de komende jaren zal het epigenoom, net als het genoom, in kaart worden gebracht. Kennis over DNA-regulerende factoren zal leiden tot nieuwe inzichten in het genoom. Onderzoek toont aan dat er belangrijke informatie kan worden opgeslagen in gebieden van het genoom waar geen eiwitcoderende genen liggen. Dit kan informatie bevatten die niet via eiwitten wordt gecommuniceerd, zoals de rol van miRNA's (microRNA's) in hematopoëse.
Men schat dat er naast de 30.000 eiwitcoderende genen, minstens evenveel genen zijn die coderen voor miRNA's, siRNA's (small interfering RNA's) of andere regulerende RNA's. Deze moleculen spelen waarschijnlijk een cruciale rol in de expressie van eiwitcoderende genen.
Chromosomen, Mutaties en Genetische Afwijkingen
DNA is georganiseerd in chromosomen, die zichtbaar zijn tijdens celdeling. Een menselijke celkern bevat 46 chromosomen: 22 paren autosomen en één paar geslachtschromosomen (XX voor vrouwen, XY voor mannen). Somatische cellen zijn diploïd (46 chromosomen), terwijl geslachtscellen haploïd zijn (23 chromosomen).
Cytogenetica en Chromosoomanalyse
Cytogenetica is de studie van chromosomen. Chromosomen bestaan uit chromatine, een complex van DNA en histonen. Euchromatine is licht gekleurd en bevat actieve genen, terwijl heterochromatine donker gekleurd is en grotendeels inactief, repetitief DNA bevat.
Karyotypering is een methode om alle chromosomen van een individu te analyseren. Voor dit onderzoek worden vaak lymfocyten uit bloed gebruikt. De cellen worden gestimuleerd tot delen en vervolgens gestopt in de metafase, wanneer de chromosomen het meest gecondenseerd zijn. G-banding, een kleuringstechniek, creëert een karakteristiek bandenpatroon voor elk chromosoom, wat helpt bij identificatie.
FISH (Fluorescent In-Situ Hybridization) maakt gebruik van fluorescerende DNA-probes om specifieke chromosoomregio's te detecteren. CGH (Comparative Genomic Hybridization) en de geavanceerdere Array CGH kunnen DNA-verlies en -uitbreidingen op genoomniveau identificeren door de fluorescentie van test-DNA te vergelijken met controle-DNA.
Mutaties: Veranderingen in het Genetisch Materiaal
Mutaties zijn overerfbare veranderingen in het genetische materiaal die evolutie bevorderen, maar ook ziektes kunnen veroorzaken. Ze kunnen ontstaan door blootstelling aan mutagene stoffen of spontaan. Somatische mutaties worden niet doorgegeven, maar mutaties in geslachtsklieren of -cellen wel.
- Substitutie: Een nucleotide wordt vervangen door een ander. Een transitie vindt plaats tussen nucleotiden van hetzelfde type (pyrimidine/purine), terwijl een transversie een pyrimidine met een purine uitwisselt.
- Deletie: Verlies van één of meerdere nucleotiden.
- Insertie: Toevoeging van één of meerdere nucleotiden.
Een dynamische mutatie treedt op wanneer een zich herhalende sequentie instabiel wordt naarmate deze langer wordt. Dit kan leiden tot ziektes die plotseling opduiken in families. Het langer worden van een dynamische mutatie over generaties heen wordt anticipatie genoemd.
Afhankelijk van het effect op het eiwit, onderscheiden we:
- Synonieme/stille mutatie: Verandert het eiwit niet.
- Niet-synonieme mutatie: Verandert het eiwit.
- Missense-mutatie: Vervangt één aminozuur door een ander.
- Nonsense-mutatie: Creëert een stopcodon, wat leidt tot een verkort eiwit.
- Frameshift-mutatie: Een insertie of deletie die niet in drievoud is, verandert het leesraam en leidt vaak tot een vervroegd stopcodon.
Mutaties in niet-coderend DNA kunnen schadelijk zijn als ze genexpressie reguleren, zoals in promotors of splicinggebieden.
Gevolgen van Mutaties
De gevolgen van mutaties kunnen zijn:
- Verlies van functie: Resulteert in een hypomorf (verminderde functie) of amorf (geen functie) eiwit. Vaak zijn deze aandoeningen recessief.
- Winst van functie: Kan leiden tot nieuwe functies of overexpressie, wat dominante ziektes kan veroorzaken.
- Dominante negatieve mutatie: Het gemuteerde gen verstoort de functie van het gezonde gen.
Genotype-fenotype correlatie koppelt specifieke genotypen aan fenotypes, wat helpt bij het inschatten van risico's voor bepaalde ziektes.
Chromosoomafwijkingen
Chromosoomafwijkingen worden onderverdeeld in numerieke en structurele afwijkingen.
Numerieke Chromosoomafwijkingen
Bij numerieke afwijkingen is er een teveel of tekort aan een of meer chromosomen.
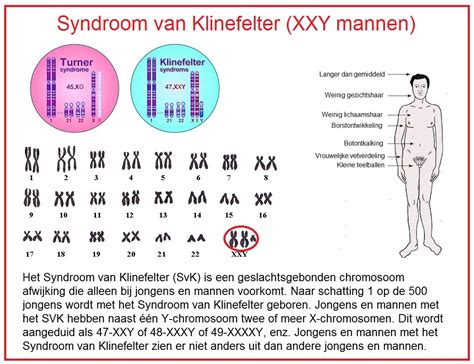
- Aneuploïdie: Een extra chromosoom (trisomie, zoals bij het syndroom van Down met trisomie 21) of een ontbrekend chromosoom (monosomie, zoals het syndroom van Turner met monosomie X). Dit ontstaat vaak door nondisjunctie tijdens de celdeling.
- Polyploïdie: Meerdere complete sets chromosomen (bijvoorbeeld triploïdie met 69 chromosomen). Dit komt vaak voor bij miskramen en kan ontstaan door bevruchting van een eicel door twee zaadcellen (dispermie).
Mozaïcisme treedt op wanneer nondisjunctie plaatsvindt tijdens vroege mitotische delingen in de zygote, wat resulteert in verschillende celijnen binnen één individu.
Structurele Chromosoomafwijkingen
Structurele afwijkingen ontstaan door het breken en reorganiseren van chromosomen.
- Translocaties: Genetisch materiaal wordt verplaatst tussen chromosomen. Bij een reciproke translocatie wisselen fragmenten tussen twee chromosomen. Een Robertsoniaanse translocatie betreft het samensmelten van twee acrocentrische chromosomen bij het centromeer.
- Deleties: Verlies van een deel van een chromosoom.
Gebalanceerde translocaties kunnen problemen veroorzaken tijdens de meiose, wat kan leiden tot ongebalanceerde varianten en miskramen of kinderen met afwijkingen.
Prenatale Screening: De NIPT
De NIPT (niet-invasieve prenatale test) kan vanaf 10 weken zwangerschap worden uitgevoerd. Deze test onderzoekt DNA dat afkomstig is van de placenta in het bloed van de zwangere. Dit DNA is bijna altijd identiek aan dat van het kind, waardoor het laboratorium kan screenen op chromosoomafwijkingen.
Niet alle zwangeren komen in aanmerking voor de NIPT; medische redenen kunnen de betrouwbaarheid van de uitslag beïnvloeden. De keuze voor een bloedafnameorganisatie is aan de zwangere, in overleg met de verloskundige of gynaecoloog.
Persoonlijke Onderzoeksachtergrond
De auteur van dit artikel, na afronding van de studie Dierwetenschappen in 2004, werkte als promovendus aan de Universiteit Maastricht, waar onderzoek werd gedaan naar de invloed van genetische factoren op type 2 diabetes bij tweelingen. Vervolgens specialiseerde de auteur zich in epigenetisch onderzoek bij eeneiige tweelingen aan de Universität des Saarlandes in Duitsland.