Slechts dertig procent van de embryo’s die ontstaan bij IVF, nestelt zich succesvol in na terugplaatsing in de baarmoeder. Vervolgens gaat het bij een kwart van de ingenestelde embryo’s alsnog mis: vrouwen krijgen aanvankelijk een positieve zwangerschapstest, maar verliezen het vruchtje twee weken later. Onderzoekers vermoeden dat dit komt door afwijkingen in het aantal chromosomen, de dragers van het erfelijke materiaal.
Onderzoek naar Succespercentages van IVF
Om te onderzoeken waarom IVF-trajecten zo vaak misgaan, gebruiken wetenschappers sinds 2021 een bepaald soort embryo-modellen: blastoïden. Blastoïden bootsen de fase van de embryonale ontwikkeling na waarin het embryo zich innestelt in de baarmoeder. Embryo’s in die zogeheten blastulafase heten blastocysten en ‘oïde’ betekent ‘achtig’. Vandaar blastoïden, omdat het om modellen gaat.
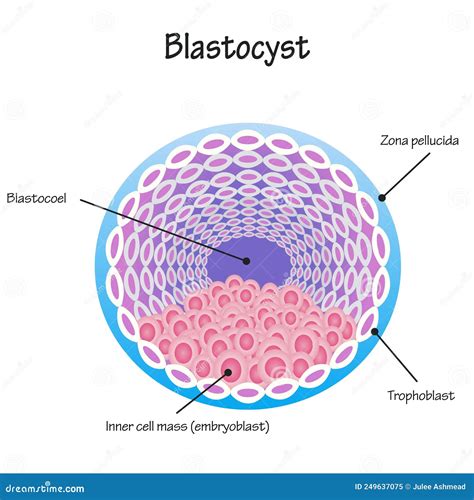
Een blastocyst ziet eruit als een klein blaasje, waarvan de buitenste laag cellen een holte omsluit waarin zich een klompje cellen bevindt. De buitenste cellaag zorgt voor de innesteling in de baarmoeder en vormt de placenta, terwijl het binnenste klompje cellen uitgroeit tot het embryo. Blastoïden moeten zo goed mogelijk op zo’n blastocyst lijken.
De Noodzaak van Embryo-Modellen
Die modellen zijn hard nodig. Zonder modellen zijn onderzoekers aangewezen op proefdieren zoals muizen als ze de vroege embryonale ontwikkeling willen bestuderen. Maar de ontwikkeling van muis en mens komt niet helemaal overeen. Muizenembryo’s ontwikkelen zich bijvoorbeeld veel sneller. De innesteling gebeurt bij mensen tussen dag 5 en 7. Bij muizen is dit al op dag 4.
Een andere optie voor onderzoekers zijn zogeheten restembryo’s die over zijn na een IVF-behandeling. Mensen die een IVF-traject doorlopen kunnen deze embryo’s aan de wetenschap doneren. Hoewel onderzoek met deze restembryo’s heel nuttig is, kleven er ook nadelen aan.
Het Creëren van Blastoïden
Als onderzoekers cellen uit de blastocyst halen en in het lab verder laten groeien, ontstaan embryonale stamcellen. Die cellen behouden het vermogen om alle embryonale weefsels te vormen. Om een humane blastoïde te maken, voegen wetenschappers die embryonale stamcellen in een buisje samen met een uitgekiende cocktail van eiwitten die de cellen stimuleren te delen en te veranderen. Zo ontstaat spontaan een bolletje dat veel lijkt op de beginfase van een embryo op dag 5 na de bevruchting, de periode waarin een embryo normaal gesproken gaat innestelen dus.
Het grote voordeel is dat onderzoekers makkelijk grote aantallen van deze modellen kunnen maken in het laboratorium. Ook kunnen ze makkelijk veranderingen in bijvoorbeeld het DNA aanbrengen om de gevolgen daarvan te onderzoeken.
Onderzoek naar Chromosomale Afwijkingen
Met blastoïden hopen wetenschappers onder andere te ontdekken welke genen bij een embryo cruciaal zijn voor een goede innesteling. Als er door afwijkingen in die genen bijvoorbeeld fouten optreden tijdens de celdeling, kunnen cellen een ongelijk aantal chromosomen krijgen. Vijftien jaar geleden ontdekten onderzoekers dat dit ongelijke chromosomenaantal vaak voorkomt in menselijke IVF-embryo’s.
Om dit te onderzoeken, gebruiken wetenschappers menselijke modellen. In tegenstelling tot wetenschappers die met muismodellen werken, plaatsen zij menselijke embryo-modellen niet terug in een baarmoeder, maar op een voedingsbodem die de baarmoederwand moet nabootsen in het lab.
Het lastige is alleen dat eigenlijk niemand weet hoe vergelijkbaar dit soort embryo-modellen zijn met echte embryo’s, en hoe nuttig ze dus zijn. Daarom worden restembryo’s doorgekweekt naar een stadium tot na de implantatie om de ontwikkeling zo goed mogelijk in kaart te brengen.
Belang van Vroege Embryonale Ontwikkeling
Onderzoekers onderzoeken de embryo’s die ze uit IVF-onderzoek krijgen op allerlei manieren om zoveel mogelijk van de ontwikkeling in kaart te brengen. Dat doen ze al vanaf de allereerste delingen die de bevruchte eicellen doormaken, de zogeheten klievingsdelingen. Sommige embryo’s hebben namelijk al direct na de bevruchting problemen.
Zulke embryo’s redden het niet als je ze terug zou plaatsen in de baarmoeder en worden normaal gesproken weggegooid. Vaak kunnen ze nog wel de ontwikkeling tot aan de innesteling doormaken en dat maakt ze geschikt voor onderzoek.
Transcriptie en de Rol van Modellen
Tijdens die eerste delingen begint ook de transcriptie, het proces waarbij DNA wordt afgelezen om uiteindelijk eiwitten te maken. Het moment dat transcriptie aangaat, kan worden gezien als de oerknal van het leven. Datzelfde onderzoek doen ze vervolgens ook met de blastoïden, modellen dus.
Het kan zijn dat die twee op bepaalde punten verschillen. Maar dat hoeft niet erg te zijn. Het zijn juist de gebreken in een model die laten zien welke factoren cruciaal zijn in de ontwikkeling. Wat gebeurt er bijvoorbeeld in het model als bepaalde eiwitten of signalen ontbreken? En op wat voor een manier verschilt dat met wat er gebeurt in het echte embryo?
IVF-Behandeling: Processen en Succespercentages
Bij een IVF-behandeling worden embryo’s traditioneel drie dagen na bevruchting teruggeplaatst in de baarmoeder. Door verbeteringen in laboratoriumtechnieken kan dit nu ook na vijf dagen. Daarvan werd aangenomen dat het de kans op een succesvolle zwangerschap verhoogt.
Eén op de dertig kinderen in Nederland is verwekt via in vitro fertilisatie, kortweg IVF. Daarbij worden eicellen buiten het lichaam bevrucht en een aantal dagen opgekweekt in het laboratorium. Vervolgens plaatst men één of meerdere embryo’s terug in de baarmoeder en vriest de rest in.
Dag 3 versus Dag 5 Embryoterugplaatsing
Traditioneel duurt de laboratoriumfase drie dagen. Door technische verbeteringen kan terugplaatsing nu ook na vijf dagen. De gedachte is dat zo alleen levensvatbare embryo’s overblijven, wat de kans op een succesvolle zwangerschap verhoogt. Eerder onderzoek wijst uit dat de kans op succes na de eerste terugplaatsing inderdaad hoger is als die plaatsvindt op dag vijf dan op dag drie.
Maar deze studies keken niet naar de resultaten van het hele IVF-traject, met eventuele latere terugplaatsingen van ingevroren embryo’s. Een studie in 21 Nederlandse IVF-centra bij ruim 1200 vrouwen vergeleek de terugplaatsing op dag drie met die op dag vijf. De uitkomst was de kans op een succesvolle zwangerschap van het hele IVF-traject.
Uiteindelijk gaat het bij IVF om een succesvolle zwangerschap, en niet alleen om de kans daarop na de eerste terugplaatsing. In het buitenland, waar IVF-zorg niet verzekerd is, maken klinieken vaak reclame met hun succespercentages van de eerste terugplaatsing op dag vijf. Daarmee geven ze een onvolledige voorstelling van zaken.
Factoren die de Keuze Beïnvloeden
Andere resultaten uit het onderzoek kunnen de beslissing voor dag 3 of dag 5 terugplaatsing beïnvloeden. Net als in eerder onderzoek was de kans op een succesvolle zwangerschap na de eerste terugplaatsing op dag vijf hoger. Ook kwamen er in die groep minder miskramen voor.
Daar tegenover staat dat er bij terugplaatsing op dag drie meer embryo’s konden worden ingevroren voor later gebruik en de kans op vroeggeboorte wat lager was. Het is een heel persoonlijke afweging. Voor de één is zo snel mogelijk zwanger worden heel belangrijk, bijvoorbeeld als de vrouw al wat ouder is. Iemand anders hecht meer waarde aan een groter aantal ingevroren embryo’s achter de hand of wil de kans op vroeggeboorte zo klein mogelijk houden. Er is geen richtlijn over de dag van terugplaatsing; dit is een gedeelde beslissing tussen arts en patiënt.
Technologische Vooruitgang in IVF
Tegenwoordig kunnen stellen met een verminderde vruchtbaarheid terecht voor een IVF-behandeling. Daarbij worden in het laboratorium enkele eicellen van de vrouw in contact gebracht met spermacellen van de man. De embryo’s die daaruit ontstaan, worden gedurende vijf dagen opgekweekt. Daarna wordt het meest geschikte embryo in de baarmoeder van de vrouw geplaatst.
De EmbryoScope en Embryo-Monitoring
Voor het kweken van de embryo’s wordt gebruik gemaakt van een EmbryoScope, een gesloten kast waarin het milieu in de eierstokken en de baarmoeder wordt geïmiteerd. De temperatuur, de zuurgraad, de zuurstof- en CO2-spanning zijn vergelijkbaar met de natuurlijke omgeving van het embryo. De EmbryoScope is bovendien uitgerust met een camera die het mogelijk maakt om de opgroeiende embryo’s gedurende langere tijd te volgen zonder ze uit hun veilige omgeving te verwijderen.
Met de EmbryoScope kan worden vastgesteld hoelang het embryo erover doet om tot een bepaald aantal cellen uit te groeien. De tijd die het kost voor een embryo om van een stadium met twee naar drie cellen te gaan, of wanneer acht cellen zijn gevormd, wordt genoteerd. De EmbryoScope maakt elke tien minuten een opname.

Selectiecriteria voor Embryo’s
In het verleden werden de embryo’s al na drie dagen bij de vrouw ingebracht. Inmiddels hebben we de kweekcondities verbeterd waardoor we de embryo’s vijf dagen kunnen kweken. Dat heeft een belangrijk voordeel. Na drie dagen was niet altijd duidelijk welk embryo het meest geschikt was om in te brengen. Er kan sprake zijn van een chromosomale afwijking, waardoor het embryo uiteindelijk niet goed doorgroeit.
Dat selecteren gebeurt nu nog zuiver visueel. Er wordt gekeken naar de vorm, de structuur en het aantal cellen. Maar er wordt ook gekeken naar andere criteria, zoals de groeisnelheid van het embryo.
Uitdagingen en Toekomstperspectieven in IVF
De kans dat een vrouw zwanger wordt met behulp van IVF ligt wereldwijd rond de 30 procent. Dat het vaak niet lukt, wordt toegeschreven aan chromosomale afwijkingen bij het embryo. Wereldwijd werken IVF-klinieken en onderzoekscentra aan verbetering van die slagingskans, onder andere door het screenen van de embryo’s op chromosomale afwijkingen.
Mosaïcisme en Genetische Afwijkingen
Het screenen op chromosomale afwijkingen is niet eenvoudig. Bij het vijf dagen oude embryo, dat dan zo’n vijftig tot honderd cellen omvat, worden vijf tot tien cellen weggenomen. Er is geen probleem als we in die cellen helemaal geen afwijkingen kunnen aantonen. Zo’n embryo zou zonder bezwaar kunnen worden geplaatst. Ook als we in álle cellen afwijkingen vinden, is de conclusie helder: dat embryo is niet geschikt.
Maar het wordt ingewikkeld als een deel van de cellen afwijkingen vertoont en een ander deel niet. Dat verschijnsel noemen we mosaïcisme. We weten nog niet goed wat we daaruit kunnen concluderen, want hoe belangrijk zijn die afwijkingen in die specifieke cel? Niet alle cellen groeien uit tot het kind, maar vormen bijvoorbeeld de placenta of de vruchtzak.
Verbetering van Succespercentages
Kind en Ten Berge willen weten hoe chromosomale afwijkingen ontstaan en hopen te ontdekken hoe deze de ontwikkelingsmechanismen van embryo’s beïnvloeden. Als dat bekend is, is een laatste stap om behandelingen te onderzoeken die een gezonde ontwikkeling bevorderen.
Als er een manier bedacht wordt om afwijkende cellen op te sporen en te verwijderen, dan kan een embryo misschien alsnog normaal ontwikkelen. Of misschien vinden we wel een manier waarop abnormale cellen stoppen met groeien, waardoor het embryo het niet redt en je dus geen embryo’s terugplaatst die toch geen kans hebben. Dit is echter nog hypothetisch. De onderzoekers zijn tevreden als ze de komende jaren meer leren over de menselijke embryonale ontwikkeling.
Statistieken en Interpretatie van IVF-Succes
De statistieken die klinieken presenteren voor IVF-succes kunnen verwarrend zijn. Het is belangrijk om te weten hoe deze percentages worden berekend.
Cumulatieve Zwangerschapspercentages
Het cumulatieve zwangerschapspercentage houdt in het aantal zwangerschappen na een eicelpunctie. Dit is inclusief een verse embryo-terugplaatsing en een mogelijke terugplaatsing van cryopreserveerde embryo’s. De leeftijd van een vrouw blijft de belangrijkste voorspeller van IVF-succes. Over het algemeen geldt: hoe jonger de vrouw, hoe hoger de kans op een succesvolle behandeling.
Verschillende Berekeningsmethoden
Veel klinieken adverteren met klinische zwangerschapspercentages, niet met levendgeborenenpercentages. Klinische vergelijkingen zijn lastig omdat klinieken variëren in de manier waarop ze succes definiëren, of ze nu bevroren cycli, PGT-gebruik of het opslaan van embryo’s meenemen.
De statistieken laten doorgaans een gemiddeld slagingspercentage tussen 30-50% zien. In de meeste klinieken worden statistieken gepresenteerd voor verschillende leeftijdsgroepen van de patiënt, waarbij de verschillen in leeftijdsafhankelijke succespercentages zeer groot kunnen zijn.
Het Belang van Transparantie
Het is cruciaal om te weten hoe de statistieken zijn berekend. IVF-succespercentages met eigen eicellen moeten worden weergegeven per leeftijd van de vrouw. De leeftijd van de vrouw heeft een beslissende invloed op de slagingspercentages van IVF; leeftijd en slagingspercentage staan lijnrecht tegenover elkaar.
De leeftijd van een vrouw is veel minder belangrijk in het geval van succes met IVF-programma’s met behulp van donoreicellen. Het moeilijkste onderdeel van het IVF-programma is het proces van het stimuleren en bevruchten van eicellen en embryo-ontwikkeling. Waarom klinieken dit deel in de statistieken van het succespercentage van behandelingen meestal overslaan, is onduidelijk.
Het IVF-Behandelingsproces
Het IVF-proces bestaat uit verschillende fasen, die elk van groot belang zijn voor het succes van het behandelprogramma.
Fasen van de IVF-Behandeling
- Kwalificatie en Voorbereiding: Beginnen met het innemen van anticonceptiemiddelen, hormonale en genetische tests, analyse van partnersperma.
- Hormonale Stimulatie: Stimulatie van de eierstokken met hormonen om meerdere eicellen te laten rijpen. FSH (follikelstimulerend hormoon) wordt gedurende zes tot vijftien dagen geïnjecteerd.
- Monitoring met Echo’s: Regelmatige echocontroles om het aantal en de grootte van de eiblaasjes te volgen.
- Uitrijpen van Eicellen: Een eenmalige injectie met Ovitrelle® (HCG) om de eicellen volledig te laten uitrijpen, ongeveer 40 uur voor de eisprong.
- Eicelpunctie: De rijpe eicellen worden via een vaginale punctie uit de eierstokken gehaald.
- Zaadproductie en Bewerking: Sperma van de partner wordt geproduceerd en in het laboratorium bewerkt.
- Laboratoriumbevruchting: De eicellen worden bevrucht met de zaadcellen. De beweeglijke zaadcellen worden gescheiden van de onbeweeglijke of afwijkende zaadcellen.
- Embryo-ontwikkeling: Na de bevruchting vinden de eerste celdelingen plaats (2-, 4- en 8-cellen). Het embryo wordt compact.
- Terugplaatsing van het Embryo: Het embryo van de beste kwaliteit wordt meestal op de derde dag na de punctie teruggeplaatst in de baarmoeder.
Periode van Afwachten en Testen
Na de terugplaatsing van het embryo volgt een periode van afwachten. Gedurende deze tijd worden progesteroncapsules (Utrogestan®) gebruikt om het baarmoederslijmvlies voor te bereiden op de innesteling. Achttien dagen na de punctie kan een zwangerschapstest worden gedaan.
Als de behandeling niet succesvol is, wordt een nagesprek met de arts gevoerd om andere behandelmogelijkheden te bespreken. Het is niet verstandig voor of na de terugplaatsing te roken, omdat roken de kans op een zwangerschap vermindert.
Factoren die Succes Beïnvloeden
Veel factoren zijn van invloed op het succespercentage van een in vitro programma met de eigen eicellen van de patiënt. De leeftijd van de vrouw is daarvan veruit de belangrijkste. De kwaliteit van de eicellen neemt af met de leeftijd van de vrouw.
Belangrijke Overwegingen
- Leeftijd van de Vrouw: De belangrijkste voorspeller van IVF-succes.
- Individuele Medische Situatie: Medische geschiedenis en specifieke vruchtbaarheidsproblemen.
- Genetische Factoren: Eventuele genetische aanleg voor vruchtbaarheidsproblemen.
- Kwaliteit van Eicellen en Sperma: Cruciaal voor succesvolle bevruchting en embryo-ontwikkeling.
- Laboratoriumprocedures: De toegepaste technieken en de kwaliteit van het laboratorium.
- Embryo-ontwikkeling: Hoe goed het embryo zich ontwikkelt na bevruchting.
- Innesteling: Het vermogen van het embryo om zich succesvol in de baarmoederwand in te nestelen.
De beste oplossing zou zijn om het verwachte succespercentage van de behandeling op een individuele manier te controleren, rekening houdend met uw leeftijd, de oorzaak van onvruchtbaarheid en andere belangrijke parameters. Online IVF-calculators kunnen hierbij helpen.
In vitro fertilisatie (IVF)
tags: #slagingspercentage #ivf #na #terugplaatsing