Wetenschappers van het Erasmus MC hebben een gen ontdekt dat een zeldzame hartspierziekte bij kinderen veroorzaakt. Ze kwamen het gen op het spoor via DNA-onderzoek bij een baby met een onverklaarde ziekte. Een op maat gemaakte zebravis bevestigde hun vermoedens.
Toen een baby van drie maanden minder goed ging drinken, werd in het Erasmus MC de oorzaak gevonden. Het kindje had de zeldzame hartziekte gedilateerde cardiomyopathie. Kinderen met die aandoening hebben een vergrote hartkamer en hun hart kan het bloed minder goed rondpompen. Hartspierziekten op kinderleeftijd zijn zeldzaam en vaak genetisch bepaald. Routine-onderzoek van bekende ziekte-veroorzakende genen levert slechts bij de helft van de kinderen een oorzaak op. Voor klinisch geneticus Judith Verhagen was dit reden voor meer onderzoek.
Het Flightless-1 Gen en zijn Rol
Het flightless-1 gen is jaren geleden ontdekt in fruitvliegen. Het gen kreeg deze naam, omdat mutaties in dit gen ervoor zorgen dat fruitvliegen niet meer kunnen vliegen. FLII speelt een rol in de spieren die nodig zijn om te vliegen. Al snel vindt het team een aanwijzing die hun vermoedens bevestigt dat de mutaties in FLII de oorzaak zijn van de hartproblemen van de baby.
Zebravissen Leveren Definitief Bewijs
Het zijn uiteindelijk zebravissen die het definitieve bewijs leveren dat de mutaties echt de oorzaak zijn van de zeldzame hartziekte bij de kinderen. Met CRISPR-Cas9 konden we zebravissen maken met exact dezelfde mutaties in het FLII-gen als de zieke kinderen. Toen Ruijmbeek inzoomde op de hartspiercellen van de vissen zag ze dat de eiwitcomplexen die zorgen dat het hart samentrekt minder goed georganiseerd zijn.
Belang voor Toekomstige Patiënten en Behandelmethoden
Dat is vooral belangrijke informatie voor toekomstige patiënten, vertelt Ruijmbeek. Als we nu een patiënt zien met onverklaarde gedilateerde cardiomyopathie kunnen genetici meteen gericht zoeken naar afwijkingen op het FLII-gen. Vanuit wetenschappelijk oogpunt is de ontdekking ook relevant, want het biedt aangrijpingspunten om te zoeken naar nieuwe, gerichte behandelmogelijkheden.
Daarbij komen de zebravissen weer om de hoek. We kunnen bijvoorbeeld potentiële nieuwe medicijnen toevoegen aan het water waarin de vissenlarven zwemmen en meten wat dat doet met de hartfunctie, legt Ruijmbeek uit.
De Historie van Zebravis Onderzoek in het Erasmus MC
De afdeling Klinische Genetica van het Erasmus MC heeft een lange historie met de zebravis. Ongeveer 20 jaar geleden kwamen de eerste visjes naar de afdeling vanuit een aquarium in een dierenwinkel. Maar toen waren de mogelijkheden nog wat beperkt. Tien jaar geleden zag toenmalig afdelingshoofd wijlen Robert Hofstra ook de potentie om de zebravissen te gebruiken voor genetisch onderzoek en zelfs diagnostiek, vertelt Tjakko van Ham. Inmiddels gebruiken we de vissen voor onderzoek waar we enkele jaren geleden alleen nog maar van konden dromen.
Eerder leidde vergelijkbaar zebravis-onderzoek ook tot ontdekkingen over de hersenziekten cerebellaire ataxie en ALSP. En er zit nog veel meer aan te komen, voorspelt Van Ham. Specifieke mutaties aanbrengen in de zebravis wordt steeds makkelijker en er blijven maar verbeterde analyse- en beeldvormingstechnieken komen.
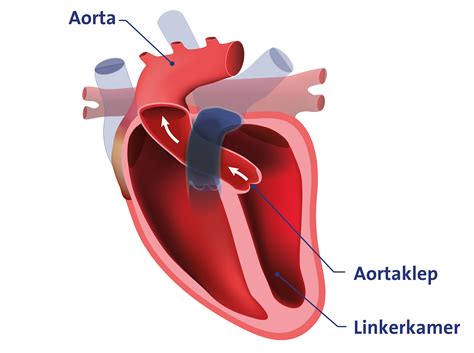
Animatie biologische hartklep
Informatiedag voor Families met Kindercardiomyopathie
Judith Verhagen organiseert samen met kindercardioloog Michiel Dalinghaus op zaterdagmiddag 18 november 2023 een informatiedag voor families met kindercardiomyopathie, met presentaties door experts, en parallelsessies waarin er ruimte is om vragen te stellen en ervaringen uit te wisselen met lotgenoten.
De Zebravis als Modelorganisme
Ontwikkeling en Kenmerken van de Zebravis
De eerste hartslag in een zebravisje-embryo vindt plaats zo’n twintig uur na de bevruchting. Het visje, Danio rerio, blijkt ook een bekend proefdier te zijn voor medisch onderzoek. Het komt oorspronkelijk uit Azië en heeft een lengte van een paar centimeters. De mannetjes zijn gewoonlijk iets kleiner en slanker dan de vrouwtjes. Door hun fellere kleuren, vinden wij ze, evenals de zebravisvrouwtjes, mooier om te zien.
De vissen planten zich zeer snel voort. De vrouwtjes leggen wekelijks een paar honderd eitjes, die zich buiten het lichaam ontwikkelen. Die doorzichtige eitjes kun je opvangen om ze onder geavanceerde microscopen te bestuderen. Zo kunnen onderzoekers de ontwikkeling van een embryo gemakkelijk bestuderen en, bijvoorbeeld, manipuleren voor genetisch onderzoek. Bovendien gaat de ontwikkeling van de bevruchte eicel tot een visje razendsnel. Het duurt vijf dagen.
Elke bevruchte eicel heeft een dooier die het embryo van voedsel voorziet. Na een kwartier begint de eicel zich te delen. Binnen vier uur zijn er duizenden cellen ontstaan. Het is wonderbaarlijk, maar na één dag ontstaan de ogen, het hart en het staartje, zijn de hersenen zichtbaar en kun je het bloed zien stromen. Maar waarom het hart ineens begint te kloppen bleef tot nu toe een raadsel.
Vergelijkingen en Verschillen met Mensen
Vanwege die snelle ontwikkeling, buiten het lichaam van de moeder, in doorzichtige eitjes, is het zebravisje een gewild en goedkoop proefdier. Toch hebben wij meer gemeen met zebravisjes dan je op het eerste gezicht zou zeggen. Als paleontoloog weet ik dat wij met de vissen zijn verbonden door een lang evolutionair proces. Als we onze stamboom terug volgen komen we ook uit bij de vissen en uiteindelijk bij het raadselachtige ontstaan van het leven op de aarde. Wat de zebravisjes en u en ik betreft, is ongeveer tachtig procent van de genen die bij ons ziekten veroorzaken, ook aanwezig in de zebravisjes, die in vele huiskamers aquaria bevolken.
Uiteraard zijn er ook verschillen. Zo hebben wij geen zwemblaas en zebravisjes wel. Evenals alle landdieren hebben wij longen. Het hart van de zebravisje is ook anders dan dat van ons. Bovendien is het spijsverteringstelsel van de zebravis anders dan dat van ons. Toch zijn er zoveel overeenkomsten dat we veel kunnen leren van het zebravis-onderzoek.
De "Levensvonk": Het Ontstaan van de Hartslag
De levensvonk, die 18-22 uur na de bevruchting plaatsvond, werd bij toeval ontdekt. De onderzoekers wilden meer leren over de communicatie tussen de cellen in een zich ontwikkelend zebravis-embryo. Hun resultaten zijn indrukwekkend. Het laboratorium beschouwt cellen, zoals in het embryo van het zebravisje, als steden en kuddes van schapen, waarin onderlinge communicatie belangrijk is. Het is die communicatie die met geavanceerde technieken in beeld wordt gebracht.
Een belangrijke focus van hun onderzoek is het bestuderen van elektrische signalen in het zenuwstelsel. Met behulp van fluorescerende eiwitten en zeer snelle microscopische beeldvorming hebben de onderzoekers veranderingen in calciumniveaus en elektrische activiteit in hartcellen van zebravis-embryo's vastgelegd. Tot hun verbazing ontdekten ze dat alle hartcellen ineens overgingen van niet-kloppen naar kloppen. Dat was te zien aan gelijktijdige pieken in de calcium- en elektrische signalen. Onmiddellijk erna begonnen de hartcellen synchroon kloppen.
De plotselinge overgang van dode cellen naar levend weefsel ontlokte Adam Cohen de opmerking “Het was alsof iemand een schakelaar had omgedraaid”. In de natuur wordt, wat je er ook van wilt denken als mens of zebravisje, diezelfde energetische schakelaar eens weer uitgezet. Dat noemen wij het einde van ons leven dat even raadselachtig is als het begin.
Zebravis Onderzoek naar Hematopoiese en Leukemie
Sasja Blokzijl-Franke, uit de groep van Jeroen den Hertog, heeft op 7 september 2021 haar proefschrift getiteld “Hematopoiese in het ontwikkelende zebravis embryo” succesvol verdedigd. Ze bestudeerde de vorming van het bloed en de invloed van verschillende factoren, waaronder PI3K-signalering, hierop. Ook deed ze onderzoek naar een mutatie in het SHP2-eiwit die betrokken is bij het ontstaan van een zeldzame vorm van leukemie bij kinderen met het Noonan Syndroom (NS), een ontwikkelingsstoornis.
Bloed voorziet het lichaam van zuurstof en voedingsstoffen, verwijdert afvalstoffen, vervoert hormonen en speelt een grote rol in de werking van het immuunsysteem. Bloed bestaat onder andere uit rode- en witte bloedcellen en bloedplaatjes. Het proces waarbij alle cellulaire componenten van bloed worden geproduceerd, wordt hematopoiese genoemd. De productie van bloedcellen wordt voornamelijk gedaan door de hematopoietische stamcel (HSC). Onderzoek naar hematopoiese wordt onder andere uitgevoerd met de zebravis als model. De embryonale ontwikkeling van zebravissen is namelijk vergelijkbaar met die van mensen. Maar er zijn ook verschillen, onder andere in de hematopoiese. Zo is in deze dieren de gespecialiseerde HSC niet te onderscheiden van zijn voorloper.
Tijdens haar promotieonderzoek bestudeerde Sasja Blokzijl-Franke de hematopoiese en de invloed van verschillende factoren hierop in de zebravis. Ze onderzocht onder meer de PI3K-signalering, die verantwoordelijk is voor de regulering van cellulaire responses zoals celdeling op externe factoren. De celdeling moet goed gereguleerd worden omdat ongecontroleerde celdeling kan leiden tot kanker. Blokzijl-Franke en haar collega’s zagen dat een deel van de HSPCs uit elkaar viel in zebravissen met een niet goed functionerend Pten-gen. Ook het remmen van PI3K-signalering in normale embryo’s leidde tot afwijkende hematopoiese. Wanneer de onderzoekers de functie van Pten herstelden of de PI3K-signalering remden, normaliseerde de hematopoiese.
Naast verder onderzoek naar de invloed van PI3K-signalering op hematopoiese, onderzocht Blokzijl-Franke ook een specifieke mutatie in het SHP2-eiwit die voorkomt bij mensen met het Noonan Syndroom (NS). NS is een ontwikkelingsstoornis met kenmerken zoals een korte lichaamslengte, hartdefecten en uitgesproken gelaatstrekken. Ook komt een zeldzame vorm van leukemie voor bij een deel van kinderen met dit syndroom. Samen met haar collega’s ontdekte Blokzijl-Franke dat een ontstekingsreactie mogelijk betrokken is bij het ontstaan van deze vorm van leukemie. Blokzijl-Franke beschrijft in haar proefschrift ook haar verdere onderzoek naar het SHP2-eiwit en zijn betrokkenheid bij PI3K-signalering en hematopoiese in zebravissen.
Zebravis Testen voor Spinale Musculaire Atrofie (SMA)
Een pasgeboren baby kan een genetische variant hebben van Spinale Musculaire Atrofie (SMA) die artsen nog niet eerder hebben gezien. Spinale Musculaire Atrofie (SMA) is een erfelijke aandoening waarbij motorische zenuwcellen langzaam verdwijnen. Dat zijn de zenuwcellen die je spieren aansturen. Het gevolg is spierzwakte en het verlies van belangrijke bewegingen, zoals slikken, zitten en uiteindelijk ook ademhalen.
Jean Giacomotto van Griffith University legt het simpel uit: “SMA zorgt voor een steeds groter verlies van motorneuronen. Daardoor worden spieren zwakker en vallen basisbewegingen weg. Voor de behandeling is timing heel belangrijk. Er bestaan inmiddels drie goedgekeurde behandelingen die het ziekteverloop kunnen veranderen, allemaal met hetzelfde doel: het lichaam meer SMN-eiwit laten maken, dat bij SMA tekortschiet. Die behandelingen werken het best als je start voordat er klachten zijn. Zodra een baby symptomen krijgt is het vaak al te laat: zenuwcellen zijn dan al onherstelbaar beschadigd.
Daar komt een lastig probleem bij: de behandelingen zijn extreem duur. Artsen proberen SMA daarom steeds vaker vroeg op te sporen via prenatale testen of de hielprik. In de meeste gevallen gaat het om bekende fouten in het SMN1-gen. Maar soms duikt er een verandering op die nog niet eerder is beschreven: een ‘variant of uncertain significance’, oftewel een VUS. Dan is de uitslag vaak onduidelijk: mogelijk is het een gevaarlijke mutatie, maar het kan ook een onschuldige variant zijn. Om die knoop sneller door te kunnen hakken ontwikkelde het team een test die gebruik maakt van zebravissen.
Het idee is verrassend praktisch. Ze gebruiken zebravis-embryo’s die geen werkend SMN-eiwit hebben. Deze larven krijgen al in de eerste week duidelijke problemen: ze ontwikkelen misvormingen, bewegen minder en sterven vroeg. Juist omdat dat allemaal zo snel gebeurt zijn ze geschikt om snel te testen of een menselijke genvariant wel of niet werkt. Voor de test verzamelen de onderzoekers eerst de SMN1-variant van de baby. Daarna injecteren ze die variant in een zebravis-embryo. Als de variant gezond genoeg is kan die het zebravisje (deels) redden: het visje ontwikkelt zich normaler, zwemt beter en overleeft langer.
Voor het onderzoek testte het team twee VUS-varianten uit de praktijk die zijn gevonden bij pasgeborenen. Tijdens de zebravistest deden deze varianten iets opvallends: ze ‘genazen’ de belangrijkste SMA-kenmerken van de larven, net zoals een ‘normale’ SMN1-variant dat doet. De volgende stap was het meest spannend. Toen de experimenten klaar waren, waren de baby’s ongeveer zes maanden oud en nog steeds zonder klachten. De artsen besloten, na overleg met de ouders, om de baby’s voorlopig niet te behandelen. Daarmee kan dit onderzoek in de toekomst hoop bieden aan ouders die een pasgeborene krijgen met mogelijk SMA.
Zebravis Model voor Amyotrofische Laterale Sclerose (ALS) Onderzoek
In het Labo Neurobiologie (Experimentele Neurologie) wordt onderzoek gedaan naar Amyotrofische Laterale Sclerose (ALS), een neurodegeneratieve ziekte. Bij ALS sterven selectief de motorische zenuwcellen af. Deze cellen verliezen daarbij hun contact met de spieren en dit leidt tot een algehele verlamming alsook tot spraakverlies. ALS is een ongeneeslijke ziekte en patiënten sterven gemiddeld 2 tot 5 jaar na het stellen van de diagnose.
De aanvangsleeftijd waarop ALS zich manifesteert, alsook de ziekteduur kunnen echter sterk verschillen van patiënt tot patiënt en dit wijst op de aanwezigheid van modificerende (genetische) factoren. In het ALS onderzoek naar deze modificerende factoren wordt er gebruik gemaakt van verschillende diermodellen. De laatste jaren is er een duidelijke kentering merkbaar waarbij het gebruik van knaagdiermodellen vervangen wordt door alternatieve modellen zoals de fruitvlieg (Drosophila melanogaster), de rondworm (Caenorhabditis elegans) en de zebravis (Danio rerio).
Zebravisembryo’s jonger dan 5 dagen oud worden verondersteld geen pijn te ervaren. Samen met de fruitvliegen vallen de zebravisembryo’s bijgevolg niet onder de wetgeving van de proefdieren. Het DNA van de zebravis vertoont 70% homologie met het menselijk DNA. Specifiek voor het onderzoek naar de ziektemechanismen bij ALS en de modificerende factoren die het fenotype kunnen beïnvloeden werd een embryonaal zebravismodel voor ALS ontwikkeld.
De avond voor het experiment worden volwassen zebravis vrouwtjes en mannetjes gescheiden. De ochtend van het experiment worden ze terug bij elkaar geplaatst in een kweekbakje waarin de vrouwtjes vervolgens kuit afzetten. Na de uitwendige bevruchting met het zaad van de mannetjes worden de eencellige eitjes verzameld. Vervolgens wordt met behulp van een micro-injectienaald ALS-gerelateerd toxisch RNA geïnjecteerd in de dooierzak. Het injecteren van verschillende condities gebeurt snel om te voorkomen dat de cellen gaan delen waardoor het RNA niet in alle dochtercellen terecht komt. Dertig uur na de bevruchting worden de embryo’s gecollecteerd. Op dit stadium is het motorisch zenuwstelsel al ontwikkeld. In het ALS zebravismodel leidt injectie van toxisch ALS-gerelateerd RNA tot kortere zenuwuitlopers en abnormale vertakkingen van de motorneuronen zoals bij patiënten met ALS. Dit fenotype wordt gebruikt als een snelle screeningsmiddel bij de zoektocht naar factoren die de ALS-gerelateerde toxiciteit kunnen verminderen. Hierbij wordt ofwel de expressie van bepaalde RNAs onderdrukt, ofwel wordt RNA coderend voor specifieke eiwitten samen geïnjecteerd met het toxische RNA. De condities waarbij de kortere zenuwuitlopers en de abnormale vertakkingen in dit zebravismodel herstellen verschaffen informatie omtrent interessante modificerende factoren.
Zebravis Embryo's voor het Testen van Medicatie-geïnduceerde Leverbeschadiging (DILI)
De lever, een belangrijk orgaan in het menselijke lichaam, maakt deel uit van het spijsverteringsstelsel en vervult vele belangrijke functies. Zo helpt de lever onder meer in het verwijderen van giftige stoffen die ontstaan tijdens de afbraak van bepaalde geneesmiddelen. De lever kan echter zelf ook beschadigd raken door deze stoffen. Meer nog, door geneesmiddelen veroorzaakte leverbeschadiging (DILI, Drug-induced liver injury) is zelfs de meest voorkomende oorzaak van leverschade (19 patiënten per 100 000 patiënten per jaar). Het is ook de belangrijkste oorzaak van acuut leverfalen met een transplantatie of overlijden tot gevolg. DILI is tevens de belangrijkste reden waarom geneesmiddelen uit de handel worden genomen.
Het laboratorium voor Moleculaire bio-ontdekking onder leiding van professor Peter de Witte ontwikkelde de methode van “Cell Imaging Counting (CIC)”. Deze techniek is gebaseerd op het gebruik van zebravisembryo’s en kent vele voordelen wat betreft het testen van hepatotoxische eigenschappen van een kandidaat-geneesmiddel. Allereerst vertonen zebravissen een grote gelijkenis met zoogdieren wat betreft de werking van de lever en de reactie van de levercellen op toxische middelen. Bovendien is de lever van de zebravis 72 uren na de bevruchting reeds volledig functioneel waardoor leverreacties vanaf een vroeg ontwikkelingsstadium kunnen opgevolgd worden. Ook biedt dit kleine organisme de mogelijkheid tot “High-throughput screening”, een proces dat geautomatiseerd testen van grote aantallen chemische en/of biologische stoffen mogelijk maakt. Zo kan één zebravispaar immers 200-300 embryo’s per week produceren waardoor embryo’s in grote aantallen ter beschikking zijn.
Bij de CIC-techniek gebruikt men zebravisembryo’s waarbij de levercellen, omwille van een genetische manipulatie, fluorescerend rood kleuren. Geneesmiddelen waarvan bekend zijn dat ze DILI veroorzaken (vb. de pijnstiller paracetamol of het antibioticum tetracycline) of nieuwe kandidaat-geneesmiddelen worden geïnjecteerd in de dooierzak van het embryo. Na drie dagen worden de embryo’s gelyseerd (het laten uiteenvallen van cellen) en de levercellen gesorteerd en geteld. Omdat de CIC-techniek wordt uitgevoerd in levende zebravisembryo’s kan men, in tegenstelling tot bijvoorbeeld testen uitgevoerd in gekweekte cellen, talrijke farmacologische kenmerken (vb.